[摘要] 城市交通的发展及其车流量的增加是社会进步的标志,但对城市的生态环境造成了严重的污染。本文主要探讨了水化环境对水泥基材料吸附重金属离子的吸附规律,研究了不同的PH值和温度下水泥基材料对重金属离子的吸附机理,并从微观结构的角度分析了具体原因。通过分析可以看出,随着PH值和温度的增加,水泥基材料对重金属离子的吸附量都呈增长趋势。
关键词:水化环境; 水泥基材料; 重金属离子; PH值和温度;吸附规律
0、 前言
城市交通的发展及其车流量的增加是社会进步的标志,但对城市的生态环境造成了严重的污染。城市交通不仅有汽车尾气的大量排放,而且有严重的重金属污染。燃油的燃烧、机油的遗漏、轮胎的磨损及金属车身和部件的剥落会产生大量的Pb、Cd、Zn等粒子(包括离子和固体微细颗粒)污染物[1]。这些污染物会沉降在道路表面,并经初期雨水冲刷后,随水流排入河流或渗入到地下水源中,进而造成城市水源的严重污染。
近年来将透水水泥基材料进行功能化改造后用于城市道路初期雨水净化处理技术有了新的发展,透水路用材料在快速排泄雨水、防止路面积水及补充地下水的同时,对初期雨水冲刷道路后携带的重金属粒子进行吸附、固定,这一分散处理技术很适合城市交通引起的无点(non-point)污染的处理。
影响水泥基材料吸附性能的因素很多,其中包括原材料的选用、集料的配比、温度以及溶液的PH值和流速等等都会影响到水泥基材料对重金属离子的吸附效果。
本论文研究的重点就是在不同的PH值和温度下,将水泥基材料浸泡在配制好的重金属离子溶液当中,经过不同的时间(3天、7天、9天),研究水泥基材料对重金属离子的吸附
规律,并通过观察其微观结构来分析吸附机理,为透水性水泥基材料的进一步研究奠定基础。
1、原材料及实验方法
1.1原材料
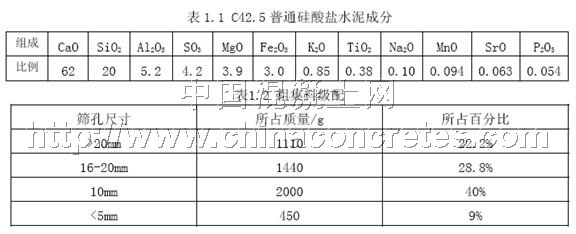
水泥:C42.5普通硅酸盐水泥,其成分分析如表1.1所示。
细集料:工业用砂
粗集料:碎卵石,其级配如表1.2所示。
水:蒸馏水
1.2 实验方法
1.2.1 配制重金属溶液对应的盐类
选用的重金属盐及其相关数据如表1.3所示:

1.2.2 配制方法
用电子天平分别称取硝酸铅4500mg、硝酸铜10872mg、硝酸锌450mg、硝酸镉4500mg,量取蒸馏水250ml,混合倒入一个洁净的烧杯中。然后将配制好的溶液,用硝酸酸化至PH<2,在25℃的温度下用恒温磁力搅拌器搅拌24小时,再将搅拌好的重金属溶液倒入装有4250ml蒸馏水的透明容器中并进行搅拌,以使重金属溶解充分[2]。然后,将水泥基材料浸泡到配制好的重金属溶液当中,在不同的PH值(PH=2、4、5.6、8)和温度(20℃、40℃、60℃、80℃)下,分别在3天、7天和9天,用胶头滴管在溶液的不同位置取溶液4~5ml,用ICP原子发射光谱仪来测定溶液中各种重金属离子的浓度。
2 实验结果及分析
2.1 实验结果
根据2.2.2实验方法,所测得的四种重金属离子在不同条件下的浓度值如表2.1所示。

2.2 分析讨论
2.2.1 PH值对重金属离子吸附的影响

|
图2.1 20℃时PH值对离子浓度的影响 |
图2.2 40℃时PH值对离子浓度的影响 |
如上图2.1和图2.2所示,除锌离子外,随着PH值的增大,溶液中重金属离子浓度总体呈下降趋势,某些离子在PH值4~6时呈现反常现象,说明水泥基材料对重金属离子的吸附作用随PH值的增大而呈增加趋势,主要是由于碱性环境有利于水泥水化,水化产物的量是决定吸附能力的主要因素。并且,在PH=8的条件下,重金属离子对应的盐类就会发生复分解沉淀反应,致使四种重金属盐在水泥基材料的微细孔内沉淀。
2.3温度对重金属离子吸附的影响

如图2.3所示,随着温度的升高,Cu2+的浓度逐渐减少,Cd2+和Pb2+的浓度总体趋势是降低的,但是中间有一个转折点,Zn2+浓度则基本不受温度的影响。由此可以看出,随着温度的升高,水泥基材料对重金属离子的吸附能力总体呈增长的趋势。主要原因是随着温度的升高,水化速度加快促使水化产物增多,且水化产物中的多聚物迅速增加[3]。多聚物的增加,促使C-S-H凝胶结构呈层状分布,有利于对重金属离子的吸附。
2.4 吸附机理讨论
利用QANTA-ZW型扫描电镜,对在不同PH值下的混凝土试块进行了微观结构分析,如图2.4~图2.6所示。

由图可以看出,PH值较低时重金属离子一般都粘附在水泥基材料的表面,主要是因为在强酸性水化环境中,水泥水化进程慢导致水化产物较少,如图2.4所示; PH=5.6的条件下,重金属离子已经进入到水泥基材料的微细孔内,并且开始发生同晶置换作用,主要是因为水泥水化产生大量的C-S-H和Ca(OH)2, 这些水化产物不但会产生大量的孔隙和比表面积,而且会产生出大量的Ca2+,如图2.5所示; PH=8时水泥基材料的表面开始出现大体积的沉淀物,这主要是由于在碱性条件下,大部分重金属离子会和OH-发生分解沉淀反应,致使大量的重金属离子沉淀在水泥基材料的微细孔表面,如图2.6所示。
综上分析可以看出,水泥基材料对重金属离子的吸附包括以下三个方面:①物理吸附。由于水化产物特别是C-S-H凝胶的高速分散性,其中又包括有数量如此众多的微细孔隙,所以硬化水泥浆体具有极大的内表面积;另外在水化过程中,水化产物的体积要大于熟料矿物的体积。据计算,每1cm3水泥水化后需占据2.2cm3空间。即约45%的水化产物处于水泥颗粒原来的周界之内,成为内部水化产物,另有55%则为外部产物,占据着原先充水的空间。这样,随着水化过程的进展,原来充水的空间减少,而没有被水化产物填充的空间,则逐渐被分割成形状不规则的毛细孔。这样产生的结果,也使水泥基材料在充分养护后产生巨大的比表面积,成为吸附重金属离子的一大因素。②复分解沉淀反应。伴随着溶液PH值的不断增大,水泥基材料的微孔隙内,重金属离子会发生复分解沉淀反应,这也是导致溶液中重金属离子浓度降低的又一原因。③同晶置换作用。水泥水化产物中Ca-Si-H凝胶为层状硅酸盐,许多重金属阳离子能置换其晶格中的Ca、Al、Si离子,从而被牢固地束缚[4]。
4 结论
(1)水泥基材料对不同的重金属离子(Cu2+、Zn2+、Pb2+、Cd2+)有选择吸附现象。
(2)除锌离子外,水泥基材料对重金属离子的吸附量,随PH值的增加和温度的升高呈递增趋势。
(3)微观结构分析表明,随着PH值的不同,水泥基材料对重金属离子的主要吸附方式也不一样。
参考文献
[1] Carolina A.Pinto,J.Dweck,J.J.Sansalone. Early stages of solidification/stabilization of storm water runoff solid residuals in cement[J].Journal of Thermal Analysis and Calorimetry.Vol.80 (2005):715-720.
[2] W.Mozgawa,T.Bajda. Spectroscopicstudy of heavy metals sorption on clinoptilolite.Phys Chem Minerals (2005) 31: 706-713.
[3] 沈威,黄文熙,闵盘荣,等.水泥工艺学[M].武汉工业大学出版社,2005,192.
[4] 管宗甫,何军志.混凝土固化废弃物中有害金属离子浸出研究[J]. 安阳师范学院学报,2007: 3.

















